本期将带您深入基因编辑正史的核心:一把源自细菌与病毒30亿年攻防战的"分子剪刀"——CRISPR/Cas9技术,它正以纳米级精度重写生命密码。这场颠覆生物医学领域的革命,其开端竟隐藏在一次被忽视的实验室意外中!
从“垃圾序列”到基因魔剪的蜕变
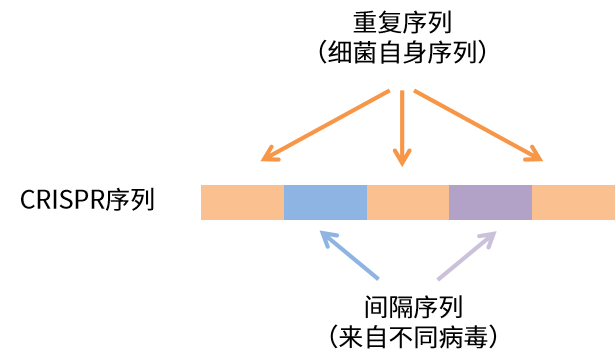
1987年,日本科学家石野良纯在解析大肠杆菌基因组中某些酶功能时,意外地在某个片段中发现了一些神秘的重复序列(即后来的CRISPR序列),但他并未深究这些看似无规律但又极具规律的片段,仅留下“值得深入探讨”几个字,因此这些奇特的序列在随后的十八年里一直沉睡于科学文献中。

神秘的重复序列(来自 Ishino, Y , et al. 1987)
此后,西班牙和荷兰等各地科学家也陆续在细菌和古细菌中发现新的重复序列,并发现这些重复序列和间隔序列的排列方式、重复序列重复出现的次数都可以表现出很大差异。因此Ruud Jansen在2002年将具有以上特征的DNA片段命名为CRISPR(Clustered Regularly Interspaced Short Palindromic Repeats,成簇规律性间隔短回文重复序列),但依旧无法解释它的作用。
直到2005年,西班牙微生物学家Francisco Mojica发表的文章才揭开了这些序列的真实身份:他证实CRISPR间隔序列匹配噬菌体DNA,提出其作为细菌“免疫记忆库”的假说。细菌通过将病毒DNA片段嵌入自身基因组,形成“分子通缉令”,当相同病毒再次来袭时,便能精准识别并摧毁入侵者。这一发现开启了基因编辑的新纪元!
2011年,Emmanuelle Charpentier团队发现CRISPR/Cas9系统的核心组分:crRNA(由CRISPR转录而来)与tracrRNA(反式激活crRNA)结合,指导Cas9蛋白切割目标DNA。
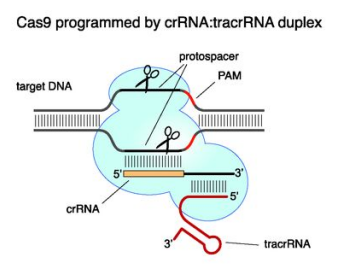
CRISPR/Cas9系统(来自Emmanuelle Charpentier,2012)
2012年,Jennifer Doudna与Emmanuelle Charpentier在《Science》发表载入基因编辑史册的里程碑研究:她们将复杂的CRISPR系统简化为Cas9蛋白+sgRNA 的二元组合,开发了第三代基因编辑工具——CRISPR/Cas9技术。只需修改sgRNA的20个碱基序列,就能引导Cas9精准切割任意DNA靶点。更因此获得了2020年的诺贝尔化学奖!

(来自诺贝尔奖官网)
次年,张锋发表了利用CRISPR技术实现哺乳动物细胞基因编辑的文章,标志着CRISPR技术从理论到实践的一大飞跃。后续科学家们的不断深入探索研究,CRISPR技术逐渐完善,正朝着基因编辑的时代迈进。
细菌免疫系统如何变身基因魔剪?
CRISPR系统的本质是RNA引导的DNA切割引擎,其纳米级精准性源于三大核心组件的精密协作:
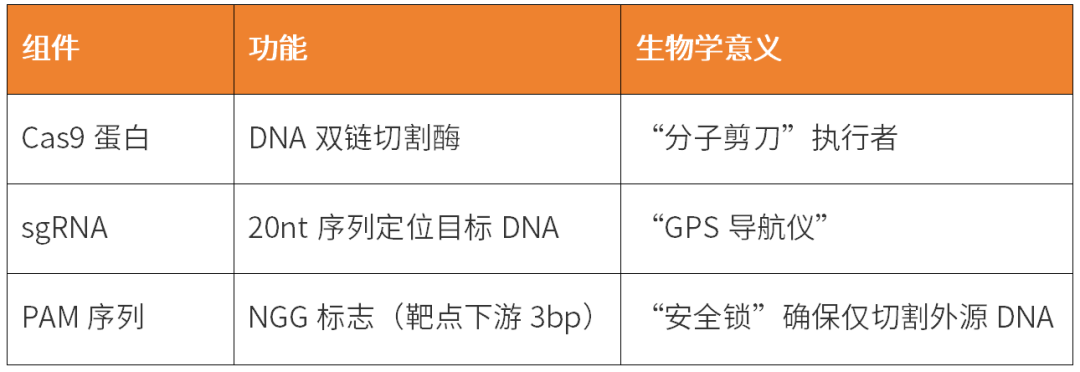
当这些组件协同工作时,将启动四步精密机制:
1.组装:Cas9与sgRNA结合形成核糖核蛋白复合体(RNP);
2.扫描:sgRNA通过碱基互补配对在基因组中搜寻目标;
3.解锁:Cas9识别PAM序列(NGG)后解旋DNA双链;
4.切割:Cas9蛋白的HNH结构域切断互补链,RuvC结构域切断非互补链。获得断裂的双链DNA(DSB)。
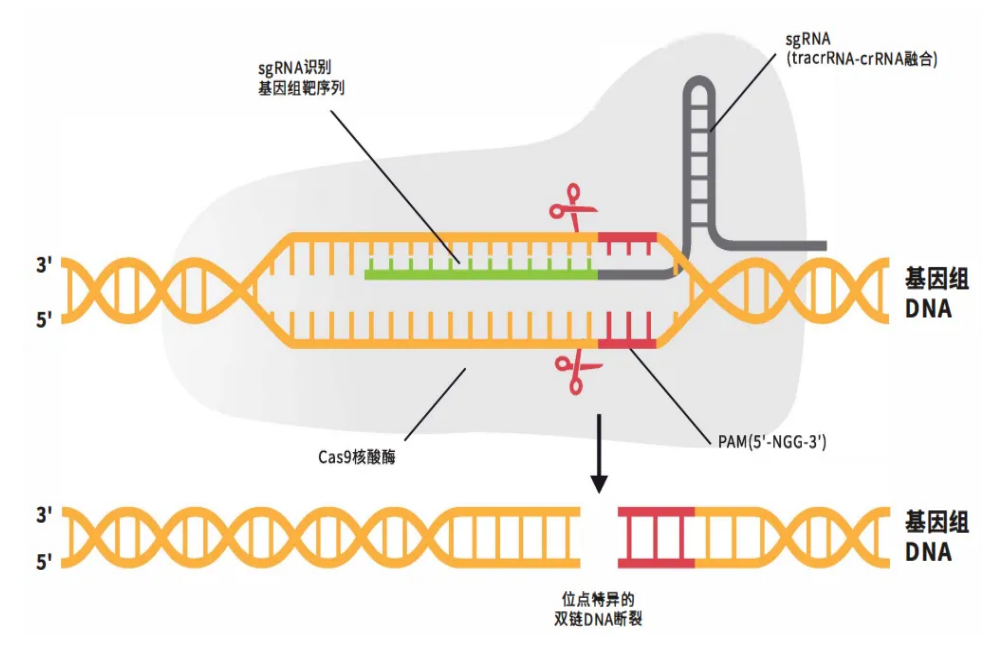
CRISPR/Cas9技术原理
切割后的DNA修复路径如下:
路径1:非同源末端连接(NHEJ),生物体内自发的SOS修复,修复期间会导致片段的插入或缺失。
路径2:同源定向修复(HDR),引入高度同源的DNA修复模板时会启动,实现片段的定向插入。
第三代技术相比于ZFNs和TALENs前两代技术更有优势,实验设计难度降低、操作流程简便、脱靶率低,细胞毒性低(如使用纯蛋白RNP体系进行基因编辑)。但依旧有脱靶风险,当sgRNA与非目标序列部分匹配时,Cas9可能误切关键基因(如癌症相关基因)。不过基因编辑研发并未止步,2023年,CRISPR基因编辑药物Casgevy上市,据2025年5月数据显示90%以上的镰状细胞病患者实现“功能性治愈”;2024年,中国科学家更发现VII型CRISPR系统(Cas14),首次实现仅靶向RNA而不改变DNA序列的精准编辑,为基因治疗开辟更安全的路径。相信在未来CRISPR技术将更加精进,运用于个性化的精准医疗,造福人类。
随着CRISPR技术从实验室走向产业化,标准化工具链的完善成为推动临床与农业应用的关键。针对基因编辑全流程的痛点——从Cas蛋白、sgRNA设计、Cas蛋白递送到脱靶验证,近岸蛋白已开发出覆盖全链条的解决方案:
01 纯蛋白编辑工具:Cas9(Cat.No.:E365)蛋白及其突变体,同时包含GMP级别的Cas9蛋白(Cat.No.:GMP-1701)、0脱靶的AaCas12bMax、enCas12Ultra等蛋白;
02 通用型一步法sgRNA制备:sgRNA体外转录试剂盒(Cat.No.:E399)在20μl体系下sgRNA产量可达10-30μg;
03 高效RNP递送系统:首先在体外将sgRNA和Cas9蛋白混合成为sgRNA和Cas9的复合效应物,然后通过瞬时转染技术(脂质体或电转等)将复合效应物递送到细胞内,进而实现对靶基因的编辑(相关实验操作可后台咨询近岸蛋白公众号);
04 脱靶验证:T7核酸内切酶I有效检测基因编辑之后形成的突变体,识别切割效率高。
三代基因编辑技术性能比对

以上便是基因编辑技术从ZFNs、TALENs到CRISPR/Cas9三代技术的进化史诗。而CRISPR革命的核心引擎——Cas蛋白家族,实则暗藏更精妙的分子江湖:下期我们将带您深入CRISPR武器库,解析不同Cas蛋白的PAM偏好、切割特性与应用场景,助您精准匹配研究需求。
作为深耕基因编辑领域的专业解决方案提供者,近岸蛋白将持续推出技术解析、实操指南与定制化工具,陪伴每一位科研工作者探索生命密码的无限可能。敬请期待,下期再会!
相关产品推荐
CRISPR/Cas9相关产品
| 产品类型 | 优势 | 目录号 | 产品名称 |
| RNA体外转录 | 通用型体外转录sgRNA | E399 | Universal sgRNA In Vitro one-step Transcription Kit |
| 一步法体外转录sgRNA | E369 | sgRNA In Vitro one-step Transcription Kit | |
| T7 RNA聚合酶转录 | E131 | T7 High Yield RNA Transcription kit | |
| SpCas9 | 通用型及突变体型 | GMP-1701 | Recombinant Cas9 Nuclease, GMP Grade |
| E365 | NLS-Cas9 Nuclease | ||
| E376 | NLS-Cas9 (D10A) Nickase | ||
| E377 | NLS-Cas9 (H840A) Nickase | ||
| E378 | NLS-Cas9 (D10A, H840A) Nuclease | ||
| E379 | NLS-Cas9-EGFP Nuclease | ||
| MR019 | Cas9 mRNA (N1-Me-Pseudo UTP) | ||
| MR107 | Cas9 mRNA | ||
|
AaCas12bMax |
零脱靶 | GMP-E375 | AaCas12bMax Enhanced, GMP Grade |
| E375 | AaCas12bMax Enhanced | ||
| MR205 | AaCas12bMax Enhanced mRNA (N1-Me-Pseudo UTP) | ||
| GR002 | AaCas12bMax Human TRAC sgRNA | ||
| GR003 | AaCas12bMax Human CIITA sgRNA | ||
| enCas12Ultra | 高编辑效率 | GMP-E393 | enCas12Ultra, GMP Grade |
| E393 | enCas12Ultra | ||
| MR208 | enCas12Ultra mRNA (N1-Me-Pseudo UTP) | ||
| piggyBac转座子mRNA | 适用于动物和人细胞的转座 | MR005 | piggyBac mRNA |
| 基因编辑效率检测 | 80倍高保真性 | E035 | 2×Fast Pfu Master Mix |
| T7核酸内切酶I | M017 | T7 Endonuclease I | |
| DNA/RNA纯化 | DNA纯化磁珠 | N240 | NovoNGS® DNA Clean Beads |
| RNA纯化磁珠 | N243 | RNA Clean Beads | |
| 病毒纯化 | GMP级 | GMP-1707 | BenzoNuclease®, GMP Grade |
| GMP-1709 | BenzoNuclease® (Tag-free), GMP Grade | ||
| GMP-1711 | High Salt Active BenzoNuclease® (HSAB), GMP Grade |
